La Food and Drug Administration degli Stati Uniti (FDA), è un’agenzia all’interno del Dipartimento della salute e dei servizi umani degli Stati Uniti, protegge la salute pubblica assicurando l’efficacia e la sicurezza dei farmaci umani e veterinari, dei vaccini e di altri prodotti biologici per uso umano e dei dispositivi medici. L’agenzia è anche responsabile della sicurezza e dell’approvvigionamento alimentare, dei cosmetici, degli integratori alimentari, dei prodotti che emettono radiazioni elettroniche e della regolamentazione dei prodotti del tabacco.
La FDA ha rilasciato un’autorizzazione all’uso di emergenza EUA (consente l’uso di prodotti non ancora approvati per trattare o prevenire malattie gravi o potenzialmente letali, come il Covid-19, in risposta a un’emergenza di sanità pubblica per la quale non esistono alternative adeguate, approvate e disponibili) per il primo test diagnostico coronavirus Covi-19 che fornisce risultati rapidi per l’autotest a casa.
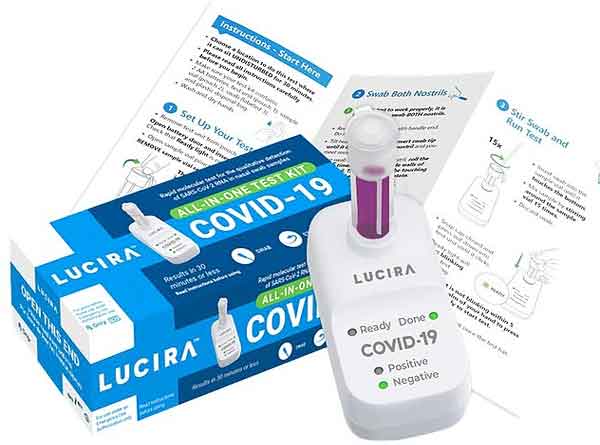
Il kit di test coronavirus Covid-19 (tutto in uno) Lucira è un test diagnostico molecolare (reazione di amplificazione mediata da loop in tempo reale) ha lo scopo di rilevare il nuovo virus SARS-CoV-2 che causa il coronavirus Covid-19. È stato autorizzato per l’uso domestico con campioni di tamponi nasali raccolti autonomamente in individui di età pari o superiore a 14 anni sospettati dal proprio medico di essere positivi al coronavirus Covid-19.
È anche autorizzato per l’uso per tutte le età in strutture punto di assistenza (POC) come studi medici, ospedali, centri di cure urgenti e pronto soccorso, ma i campioni devono essere prelevati da un operatore sanitario quando il test è utilizzato presso il POC per testare individui di età inferiore ai 14 anni. Il test è attualmente autorizzato solo per uso su prescrizione.
Il test Lucira funziona facendo roteare il tampone in ogni narice cinque volte. Il tampone viene poi mescolato nel contenuto chimico di una fiala, e poi premuto nell’unità per avviare il test. I risultati in 30 minuti o meno, possono essere letti direttamente dal display luminoso dell’unità di test, mostra se una persona è positiva o negativa per il virus SARS-CoV-2. I risultati positivi indicano la presenza di SARS-CoV-2. Gli individui con risultati positivi dovrebbero autoisolarsi e cercare cure aggiuntive dal proprio medico. Gli individui che risultano negativi e manifestano sintomi simili al coronavirus Covid-19 dovrebbero seguire il proprio medico curante poiché i risultati negativi non precludono un individuo dall’infezione da SARS-CoV-2.
La capacità di tracciare e monitorare in modo efficiente i risultati è una componente importante per il successo dei test a casa. Gli operatori sanitari prescrittori, come indicato nell’autorizzazione all’uso di emergenza (EUA), sono tenuti a riportare alle autorità sanitarie pubbliche competenti in conformità con i requisiti locali, statali e federali, tutti i risultati che ricevono dalle persone che utilizzano il kit di test. Lucira Health, il produttore del test, ha anche sviluppato l’etichettatura delle scatole, istruzioni di riferimento rapido e istruzioni per gli operatori sanitari per assistere con la segnalazione.
I test diagnostici rimangono uno dei pilastri della risposta delle nazioni al coronavirus Covid-19. La FDA continua il suo impegno per la salute pubblica a perseguire nuovi metodi che aiutano a rendere disponibili i test a più americani attraverso l’autorità dell’EUA.